

使用的样品采集器
检验系统和设备(例如血液分析、体液分析、分子诊断和免疫诊断)
细胞和组织基因检测制品
包括基因组学
转录组学
蛋白质组学和代谢组学制品等等。
-
能否确保出证?认证中会有哪些阻碍?
-
价格可信吗?是否存在隐形收费?
-
多久能出证?能否确保及时出证?
-
流程复杂吗?就怕耽误日常工作!
-
IVDR法规的主要要求
(1)注重质量管理
IVDR规定,所有生产厂家必须建立一个严格的质量管理系统,该系统必须覆盖整个生产周期,从研发、设计、生产、包装、标签、储存、分销到售后的每一个环节。
(2)进行临床验证
生产厂家必须在 CE 认证前进行临床验证,以证明其产品的性能和安全性。
(3)实行风险管理
生产厂家必须采用科学的风险管理方法,对潜在的风险进行评估和避免。这对于产品从原材料采购到生产出厂之前都必须进行。
(4)加强技术文档的管理
IVDR规定,生产厂家必须建立和保持技术文档档案,并及时更新。这些文档必须包括产品证明文件、产品标识等一系列的文件。
-
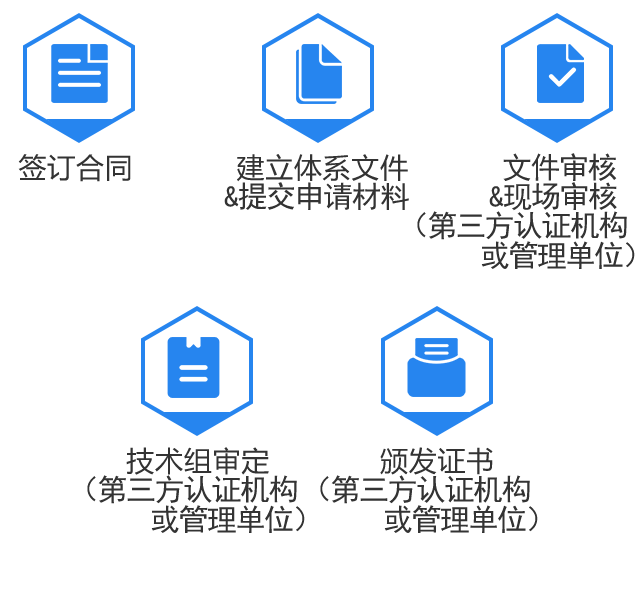
医疗器械CE认证所需程序及流程
(一)确认出口国家
(二)确认产品类别及欧盟相关产品指令
(三)指定“欧盟授权代表( 欧盟授权代理 ) ”(Authorized Representative)
(四)确认认证所需的模式(Module)
(五)采用 " 自我声明 " 模式还是 " 必须通过第三方认证机构"
(六)建立技术文件 (Technical Files) 及其维护与更新
-
医疗器械CE认证分类
Class I other 1类其他
Class I sterile 1类灭菌
Class I measurement function 1类测量
Class IIa 2a类
Class IIb 2b类
Class III and Class III with medicine 3类及3类带药物

亿荣达-认证验厂咨询部辅导老师,是由注册审核员、咨询老师、培训老师,和有机检查员,或农业科技公司、农业大学和种植、养殖、加工专业技术人员和企业质量、生产、技术、检验、管理等人员提供的。
亿荣达服务客户覆盖:黑龙江、吉林、辽宁、内蒙等18个省和自治区。
-

认证顾问
提供前期认证咨询
-

项目跟进
您的全程验证管家
-

咨询师
专业咨询铁军团队
-

售后维护
贴心服务全程安全

 咨询热线 13136680305
咨询热线 13136680305
申诉/售后:0451-58973181 业务合作:18646310958
工作日: 8:20 - 17:20
Copyright © 2024 哈尔滨亿荣达检验技术有限公司
备案号:黑ICP备19006382号






